健康診断で「LDLコレステロールが高いですね」と指摘されたこと、ありませんか? LDLコレステロールは「悪玉コレステロール」とも呼ばれ、自覚症状がないまま全身の血管を傷つけ、心筋梗塞・脳梗塞・認知症・閉塞性動脈硬化症など命に関わる病気を引き起こします。 世界の心血管疾患(脳卒中や心臓疾患など)による死亡の約半数に高LDLコレステロールが関与しています。 NEJM・The Lancet・Nature Medicineなど近年の研究論文をもとに、脳神経外科専門医が「LDLコレステロールが体に何をしているのか」と「今日からできる予防法・最新治療」を網羅的に解説します。
😄ちょこっと解説‼️
1995年に導入されたICD-10では、脳卒中は「心血管疾患」として心臓や血管の病気と同じグループに分類されていました。 2027年に導入予定のICD-11では、脳卒中は神経系の病気のグループへ移ります。 脳卒中は血管が詰まったり破れたりして起こりますが、最終的に傷つくのは脳(神経)であるため、当然ではあるのですが、「神経の病気」として扱う方が実態をより正確に反映していると判断されたためです。 ですので、現時点で脳卒中は、日本においては心血管疾患に含まれます。
このブログの目次
監修:我妻敬一(脳神経外科専門医・脳卒中専門医)
大阪市天王寺区 あづま脳神経外科リハビリクリニック 院長 脳神経外科臨床経験25年以上
このブログのポイント!
- LDLコレステロールも「サイレント・キラー」です。 自覚症状がないまま、全身の動脈硬化を進行させます。 世界で年間440万人以上が高LDLコレステロールに関連する心血管疾患で死亡しています。
- 動脈硬化のメカニズム: LDLが血管壁に侵入→ プラーク形成→ 破裂して血栓化→ 血管閉塞という段階で進行します。
- 心筋梗塞・狭心症の最大のリスク因子のひとつがLDLコレステロールです。 LDLが約39mg/dL下がると、心血管疾患の発生率が約22%減少します(CTTメタ解析)。
- アテローム血栓性脳梗塞の原因となる頚動脈プラークの形成・進行にLDLコレステロールが深く関与しています。 Treat Stroke to Target試験(NEJM 2020)では、LDL<70mg/dLへの厳格な管理で脳卒中再発リスクが22%低下しました。
- 認知症の新たなリスク因子として、2024年Lancet委員会が高LDLコレステロールを追加しました。 全認知症の約7%が中年期の高LDLコレステロール血症に起因すると推定されています。
- 閉塞性動脈硬化症(PAD)は世界で2億3,000万人以上が罹患しており、LDLコレステロールは主要なリスク因子です。 足の血管が詰まり、歩行困難や壊疽につながります。
- 治療の柱はスタチンです。 これに加え、エゼチミブ・PCSK9阻害薬・ベムペド酸など新しい治療薬も登場し、LDLをさらに低下させることが可能になりました。
- 2025年ESC/EASガイドラインでは、超高リスク患者のLDL目標値を40mg/dL未満とする「extreme risk」カテゴリが新設されました。 「低ければ低いほど良い(Lower is Better)」が世界の潮流です。
第0章 LDLコレステロールとは?
皆さん、健康診断の結果で「LDLコレステロールが高い」と言われて、どう思いましたか? 「まあ、特に症状もないし、大丈夫だろう……」と、そのまま放置していませんか?
実は、その「症状がない」ことこそが、LDLコレステロールの最も恐ろしい特徴なのです。 高血圧が「サイレント・キラー」と呼ばれるのと同じように、高LDLコレステロールも「サイレント・キラー」として振る舞い、自覚症状がまったくないまま、何年も何十年もかけて、全身の血管を静かにむしばんで行くのです。
世界で年間440万人もLDLコレステロールが原因で亡くなっている!
2022年にBMC Public Healthに発表されたGlobal Burden of Disease(GBD)Study 2019のデータ解析では、高LDLコレステロールに起因する死亡は世界で年間約440万人に達し、1990年の約310万人から大幅に増加しています。 心血管疾患全体の死亡数1,920万人(2023年GBD)のうち、高LDLコレステロールは高血圧・食事リスクとともに最も寄与の大きい修正可能なリスク因子として位置づけられています。
さらに衝撃的なのは、高コレステロール血症の約75%の患者さんがLDL目標値を達成できていないという報告です。 つまり、世界中の高コレステロール血症の方の4分の3が、十分な治療ができていないのです。
そもそもLDLコレステロールとは?
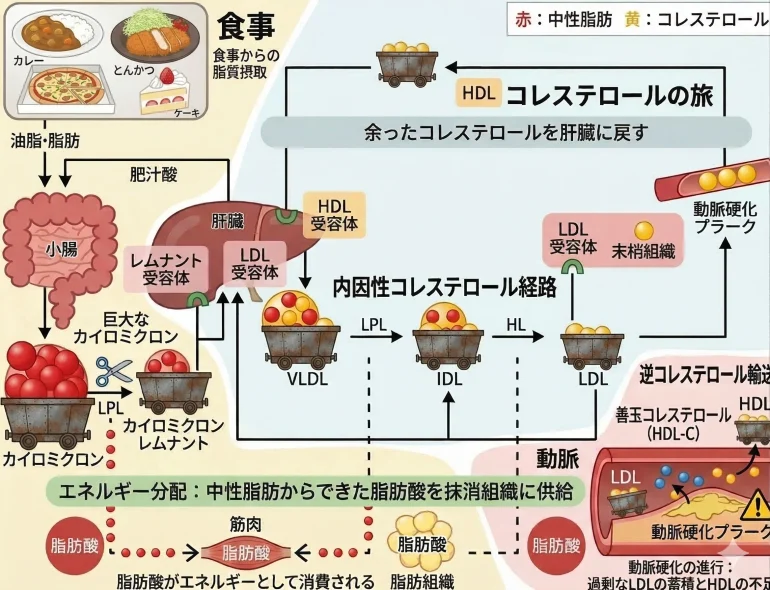
コレステロールは、体にとって必要不可欠な物質です。 体を形作っている一つひとつの細胞の骨格である細胞膜の材料で、ホルモンやビタミンDの合成などにも使われています。 コレステロールは水に溶けないため、「リポタンパク質」という運搬カプセルに包まれて血液中を移動します。
このうち、肝臓から体の各細胞にコレステロールを届ける役割を担うのがLDL(Low-Density Lipoprotein:低比重リポタンパク質)です。 一方、細胞で余ったコレステロールを回収して肝臓に戻す役割を担うのがHDL(High-Density Lipoprotein:高比重リポタンパク質)で、「善玉コレステロール」と呼ばれています。
LDLは本来、体に必要なコレステロールを届ける大切な仕事をしていますが、血液中のLDLが多すぎると問題が起こります。 余ったLDLが血管の壁の内側に入り込み、動脈硬化を引き起こすのです。
動脈硬化のメカニズム
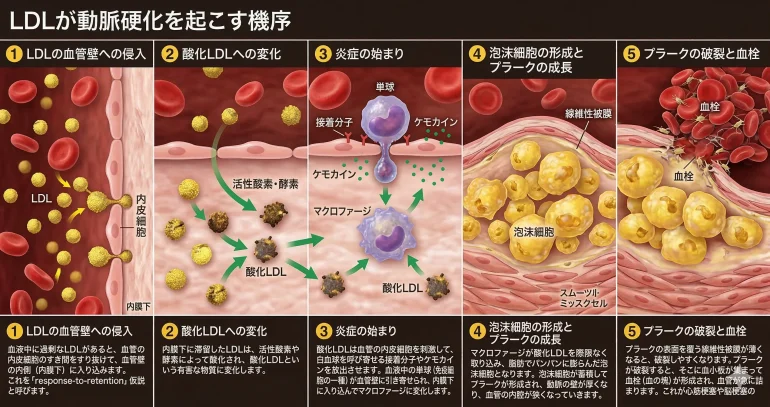
2020年に欧州動脈硬化学会(EAS)がLDLと動脈硬化の因果関係に関するエビデンスを包括的にまとめて発表しました。 この論文で、動脈硬化がどのように始まり進行するのかが明確に整理されています。
- LDLの血管壁への侵入: 血液中に過剰なLDLがあると、血管の内皮細胞のすき間をすり抜けて、血管壁の内側(内膜下)に入り込みます。 これを「response-to-retention(滞留に対する応答)」仮説と呼びます。
- 酸化LDLへの変化: 内膜下に滞留したLDLは、活性酸素や酵素によって酸化され、酸化LDLという有害な物質に変化します。
- 炎症の始まり: 酸化LDLは血管の内皮細胞を刺激して、白血球を呼び寄せる接着分子やケモカインを放出させます。 血液中の単球(免疫細胞の一種)が血管壁に引き寄せられ、内膜下に入り込んでマクロファージに変化します。
- 泡沫細胞の形成とプラークの成長: マクロファージが酸化LDLを際限なく取り込み、脂肪でパンパンに膨らんだ泡沫細胞となります。 泡沫細胞が蓄積してプラークが形成され、動脈の壁が厚くなり、血管の内腔が狭くなっていきます。
- プラークの破裂と血栓: プラークの表面を覆う線維性被膜が薄くなると、破裂しやすくなります。 プラークが破裂すると、そこに血小板が集まって血栓(血の塊)が形成され、血管が急に詰まります。 これが心筋梗塞や脳梗塞の発症メカニズムです。
つまり、LDLコレステロールが高い状態が続くと、血管の壁の中で「慢性的な炎症」が静かに進行し、ある日突然破裂して、心筋梗塞や脳梗塞として発症するのです。
😄ちょこっと解説‼️
LDLコレステロールと高血圧は、動脈硬化を促進する「最悪コンビ」です。 高血圧による血管壁へのストレスがLDLの侵入を助け、LDLによるプラーク形成が血管を狭くしてさらに血圧を上げる。 この2つの疾患が揃うと、動脈硬化は加速度的に進行します。 当院のブログ:高血圧と脳卒中・認知症の関係|脳神経外科専門医が最新エビデンスで解説もぜひご覧ください。
📖 根拠文献: Ference BA, Ginsberg HN, Graham I, et al. Low-density lipoproteins cause atherosclerotic cardiovascular disease. 1. Evidence from genetic, epidemiologic, and clinical studies. A consensus statement from the European Atherosclerosis Society Consensus Panel. Eur Heart J. 2017;38(32):2459–2472.
📖 Borén J, Chapman MJ, Krauss RM, et al. Low-density lipoproteins cause atherosclerotic cardiovascular disease: pathophysiological, genetic, and therapeutic insights: a consensus statement from the European Atherosclerosis Society Consensus Panel. Eur Heart J. 2020;41(24):2313–2330.
📖 Zhong P, Wu S, Feng R, et al. The Global Burden of Diseases attributed to high low-density lipoprotein cholesterol from 1990 to 2019. BMC Public Health. 2022;22:1903.
📖 Global Burden of Disease Study 2023. The Lancet. 2025;405(10498).
第1章 LDLと狭心症・心筋梗塞
心筋梗塞とは、心臓に血液を送る冠動脈が血栓で完全に詰まり、心臓の筋肉が壊死してしまう病気です。 狭心症は、冠動脈が狭くなって心臓への血流が一時的に不足し、胸の痛みや圧迫感が出る状態です。 これらを合わせて冠動脈疾患(CAD)と呼び、世界で年間約700万人が冠動脈疾患で亡くなっています。
そして、冠動脈疾患の発症に最も強く関与しているリスク因子が、LDLコレステロールです。
LDLを下げれば心筋梗塞は防げる(CTTメタ解析)
LDLコレステロールを下げることで心血管イベントが予防できるという、最も強力なエビデンスを提供しているのが、CTT(Cholesterol Treatment Trialists' Collaboration)の一連のメタ解析です。
CTTは、オックスフォード大学を中心に、スタチン治療に関する大規模ランダム化比較試験の個人レベルデータを統合して解析するプロジェクトです。 2010年にThe Lancetに発表された26試験・17万人のメタ解析では、次の重要な結論が得られました。
LDLコレステロールを約39mg/dL低下させるごとに、
主要心血管イベント(心筋梗塞・脳卒中など)のリスクが約22%低下する。
しかも、この効果は性別・年齢・糖尿病の有無にかかわらず、一貫して認められました。 さらに、より積極的にLDLを下げるほど、さらに大きなリスク低下が得られることも示されました。
| LDL低下幅 | 主要心血管イベントのリスク低下 |
|---|---|
| 約39mg/dL低下 | 約22%低下 |
| 約78mg/dL低下 | 約40%低下 |
2017年にNEJMに発表されたFOURIER試験では、スタチン治療中の心血管疾患患者27,564人にPCSK9阻害薬を追加したところ、LDLが中央値30mg/dLまで低下し、主要心血管イベントが15%低下、心血管死・心筋梗塞・脳卒中の複合エンドポイントが20%低下しました。
同じく2018年にNEJMに発表されたODYSSEY OUTCOMES試験では、急性冠症候群後の患者18,924人にPCSK9阻害薬を投与してLDLを下げることで、主要心血管イベントの有意な低下が確認されました。
さらに2025年にNEJMに発表されたVESALIUS-CV試験で、心筋梗塞や脳卒中の既往がない動脈硬化または糖尿病の患者さんにおいても、積極的にLDLを下げることで、初回心血管イベントのリスクを有意に低下させることが示されました。
これらの結果は、「LDLは低ければ低いほど良い(Lower is Better)」という原則を、さらに強く裏付けるものであり、二次予防だけでなく、一次予防にも有効である可能性を示す重要なエビデンスです。
📖 根拠文献: Cholesterol Treatment Trialists' (CTT) Collaboration. Efficacy and safety of more intensive lowering of LDL cholesterol: a meta-analysis of data from 170,000 participants in 26 randomised trials. The Lancet. 2010;376(9753):1670–1681.
📖 Sabatine MS, Giugliano RP, Keech AC, et al. Evolocumab and Clinical Outcomes in Patients with Cardiovascular Disease (FOURIER). N Engl J Med. 2017;376(18):1713–1722.
📖 Schwartz GG, Steg PG, Szarek M, et al. Alirocumab and Cardiovascular Outcomes after Acute Coronary Syndrome (ODYSSEY OUTCOMES). N Engl J Med. 2018;379(22):2097–2107.
📖 Nicholls SJ, et al. Evolocumab in Patients without a Previous Myocardial Infarction or Stroke (VESALIUS-CV). N Engl J Med. 2025.
第2章 LDLとアテローム血栓性脳梗塞
脳梗塞には高血圧が主原因であるラクナ梗塞と、心房細動など心臓疾患が原因の心原性脳塞栓症、そして、LDLコレステロールが最も深く関与するアテローム血栓性脳梗塞があります。
アテローム血栓性脳梗塞とは?
アテローム血栓性脳梗塞は、頚動脈(首の太い動脈)や脳の主幹動脈にアテローム性動脈硬化(プラーク)が形成され、そのプラークが破裂したり、血管が高度に狭窄したりすることで血流が途絶え、脳の組織が壊死する病気です。 脳梗塞の約20%がこのタイプに分類されます。
第0章で説明した動脈硬化のメカニズムが、まさに頚動脈や脳血管で起きて生じる脳梗塞が、アテローム血栓性脳梗塞です。 LDLコレステロールが高い状態が続くと、頚動脈の分岐部にプラークが徐々に蓄積し、ある日突然プラークが破裂して血栓を形成して、脳への血流が途絶え、脳梗塞が発症します。
LDLの値が高いほど、脳梗塞の発症リスクは高まる
久山町研究では、LDLコレステロール値が高いほど、アテローム血栓性脳梗塞の発症率が有意に上昇することが示されています。 さらに、ラクナ梗塞の発症率もLDLレベルと正の相関を示しています。
これは、高血圧がラクナ梗塞の「最大の原因」であるのに対し、LDLコレステロールはアテローム血栓性脳梗塞の原因であり、かつラクナ梗塞のリスクも高めるという、二重の危険性を持つことを意味しています。
脳梗塞後の再発予防におけるLDL管理(TST試験)
脳梗塞後のLDLコレステロール管理がどれほど重要かを示した画期的な臨床試験が、2020年にNEJMに発表されたTreat Stroke to Target(TST)試験です。
この試験は、フランスと韓国で実施され、アテローム性動脈硬化を伴う虚血性脳卒中またはTIA(一過性脳虚血発作)の患者2,860人を対象に、LDLコレステロールの目標値を「70mg/dL未満」とする群と「90〜110mg/dL」とする群に無作為に割り付けて比較しました。
| アウトカム | LDL<70mg/dL群 | LDL 90〜110mg/dL群 | ハザード比 |
|---|---|---|---|
| TST本体 主要心血管イベント (観察期間:3.5年) |
8.5% | 10.9% | 0.78(22%低下) |
| TST(フランスのみ版) 主要心血管イベント (観察期間:5.3年) |
9.6% | 12.9% | 0.74(26%低下) |
つまり、脳梗塞を起こした後にLDLを70mg/dL未満まで厳格に下げると、主要心血管イベント(虚血性脳卒中、心筋梗塞、緊急の頸動脈/冠動脈血行再建、心血管死の複合)が22〜26%も低下したのです。 韓国が中央値2.0年間であったため、より長く続けたフランスだけの追跡では、より主要心血管イベントが抑制されており、30人に1人の割合で次の脳卒中や心筋梗塞を防ぐことができた計算になります(NNT=30)。 しかも、脳内出血の増加は認められませんでした。
この結果は、脳梗塞の二次予防において、LDLコレステロールの厳格な管理が極めて重要であることを明確に示しています。 ですので、脳梗塞を起こされた患者さんは、LDLの目標値を70mg/dL未満が望ましいと考えています。
📖 根拠文献: Amarenco P, Kim JS, Labreuche J, et al. A Comparison of Two LDL Cholesterol Targets after Ischemic Stroke (Treat Stroke to Target). N Engl J Med. 2020;382(1):9–19.
📖 Amarenco P, et al. Benefit of Targeting a LDL (Low-Density Lipoprotein) Cholesterol <70 mg/dL During 5 Years After Ischemic Stroke. Stroke. 2020;51(4):1231–1234.
📖 Imamura T, Doi Y, Arima H, et al. LDL Cholesterol and the Development of Stroke Subtypes and Coronary Heart Disease in a General Japanese Population: The Hisayama Study. Stroke. 2009;40(2):382–388.
第3章 LDLと認知症
「LDLコレステロールが心臓や脳の血管に悪い」ことは、今や誰もが知っていることでしょう。 しかし、LDLコレステロールが認知症のリスクにもなることは、意外と知られていません。 実は、2024年に画期的な発表がありました。
2024年 Lancet委員会・・・高LDLコレステロール血症を新たな認知症リスク因子に追加
2024年にThe Lancetに発表された認知症予防に関するLancet委員会報告書(Lancet Commission 2024)は、認知症予防のエビデンスを包括的にまとめた、国際的にも評価の高い研究報告書です。 この報告書については、当院のブログ:認知症の45%は予防可能|脳神経外科専門医が伝える10の提言で、すでに紹介していますので、興味がある方は読んでおいてください。
2020年の報告では12のリスク因子でしたが、2024年の報告書ではリスク因子が14個に拡大されました。 新たに追加されたリスク因子が、「高LDLコレステロール血症」と「未治療の視力低下」でした。
Lancet委員会は、全認知症の約7%が中年期(40〜65歳頃)からの高LDLコレステロール血症に起因すると推算しています。 これは、14のリスク因子の中で難聴(7%)と並んで最も大きな寄与率です。 つまり、高LDLコレステロール血症は認知症の修正可能なリスク因子として、最も重要なもののひとつに位置づけられたのです。
| ライフステージ | リスク因子(寄与率) |
|---|---|
| 若年期〜 | 教育歴の低さ(5%) |
| 中年期〜 | 難聴(7%)・高LDLコレステロール(7%)・頭部外傷(3%)・うつ病(3%)・高血圧(2%)・運動不足(2%)・糖尿病(2%)・喫煙(2%)・過度の飲酒(1%)・肥満(1%) |
| 高齢期〜 | 社会的孤立(5%)・大気汚染(3%)・視力低下(1%) |
なぜLDLコレステロールが認知症を引き起こすのか?
LDLコレステロールが認知症リスクを高めるメカニズムには、複数の経路が考えられています。
まずは、脳血管の動脈硬化です。 LDLコレステロールによる動脈硬化が脳血管で進行すると、脳の血流が慢性的に低下します。 これにより、MRIで検出される白質病変(大脳白質の変性)や無症候性脳梗塞(隠れ脳梗塞)が蓄積し、脳のネットワークが徐々に分断されて血管性認知症へと進行していきます。
さらに注目されているのは、LDLコレステロールがアルツハイマー型認知症のリスクも高める可能性です。 高コレステロール状態は、血液脳関門(BBB)の機能障害を引き起こし、脳内のアミロイドβタンパク質(アルツハイマー病の原因物質のひとつ)の排出を妨げて蓄積を促進する可能性が示唆されています。 つまり、LDLコレステロールは血管性認知症だけでなく、アルツハイマー型認知症の発症にも関与している可能性があるのです。
Lancet委員会は、認知症予防のために40歳頃から高LDLコレステロール血症を検出し、治療することを推奨しています。 中年期からのLDLコレステロール管理が、将来の認知機能を守る上で極めて重要だということです。
📖 根拠文献: Livingston G, Huntley J, Liu KY, et al. Dementia prevention, intervention, and care: 2024 report of the Lancet standing Commission. The Lancet. 2024;404(10452):572–628.
📖 Ference BA, Ginsberg HN, Graham I, et al. Low-density lipoproteins cause atherosclerotic cardiovascular disease. 1. Evidence from genetic, epidemiologic, and clinical studies. Eur Heart J. 2017;38(32):2459–2472.
第4章 LDLと閉塞性動脈硬化症
これまで心臓と脳への影響を見てきましたが、LDLコレステロールによる動脈硬化は、足の血管にも深刻な影響を及ぼします。
閉塞性動脈硬化症とは?
閉塞性動脈硬化症(PAD:Peripheral Artery Disease、末梢動脈疾患)は、主に下肢の動脈にアテローム性動脈硬化が起こり、血管が狭くなったり詰まったりして、足への血流が低下する病気です。 世界で2億3,000万人以上が罹患しており、高齢化とともに増加しています。
PADの典型的な症状は間欠性跛行(かんけつせいはこう)です。 「歩いていると足が痛くなったり、だるくなったりして歩けなくなり、しばらく休むとまた歩けるようになる」といった症状が特徴的です。 進行すると、安静時にも痛みが出たり、足の傷が治らなくなったり、最悪の場合は壊疽(えそ)を起こして切断しないといけなくなることもあります。
ただし、この症状は腰部脊柱管狭窄症でも起きるので、鑑別が必要な場合があります。 当院では腰部脊柱管狭窄症と閉塞性動脈硬化症に対して、症状や神経所見、またMRIやABI検査で鑑別して治療しています。
LDLコレステロールはPADの主要リスク因子
PADの発症メカニズムは、冠動脈疾患や脳梗塞と基本的に同じです。 LDLコレステロールが足の動脈壁に侵入し、酸化LDLとなって炎症を惹起し、プラークが形成されて血管が狭窄していきます。
LDLコレステロールの上昇は、喫煙・糖尿病・高血圧とともにPADの最も重要な修正可能なリスク因子のひとつです。 しかし、PADの患者さんにおけるLDLコレステロールの治療達成率は極めて低いのが現状です。 日本動脈硬化学会の2022年ガイドラインの基準で、スタチン処方率はわずか34%、LDL目標値の達成率も約半数にとどまっています。
PADは「全身の動脈硬化のサイン」
ここで特に強調したいのは、PADは単なる「足の病気」ではないということです。 足の血管に動脈硬化が起きているということは、心臓の血管(冠動脈)や脳の血管にも同じ動脈硬化が進行している可能性が高いのです。
実際、PADの患者さんは冠動脈疾患や脳卒中を合併するリスクが非常に高く、PAD患者の死因の多くは心筋梗塞や脳卒中です。 つまり、足の症状(間欠性跛行など)は、全身の動脈硬化を知らせるサインなのです。
「歩くと足が痛くなる」 「足が冷たい」 「足の傷が治りにくい」 ・・・このような症状がある方は、足の血管の問題だけでなく、心臓や脳の血管のチェックも必要です。 当院ではMRI検査により、脳血管の評価と頚動脈の動脈硬化の評価を行うことができます。
📖 根拠文献: Song P, Rudan D, Zhu Y, et al. Global, regional, and national prevalence and risk factors for peripheral artery disease in 2015: an updated systematic review and analysis. The Lancet Glob Health. 2019;7(8):e1020–e1030.
📖 Lipid Management in Peripheral Artery Disease: A Focus on Recent and Evolving Data. American College of Cardiology Expert Analysis. 2024.
📖 Takahara M, et al. The real-world data of lipid-lowering treatment in patients with peripheral artery disease. J Atheroscler Thromb. 2023.
第5章 LDLコレステロールの予防と治療
ここまで、LDLコレステロールが心筋梗塞・脳梗塞・認知症・閉塞性動脈硬化症にどれほど深刻な影響を与えるかを見てきました。 では、LDLコレステロールを下げるためには、具体的に何をすればよいのでしょうか?
① 食事療法: 「飽和脂肪酸」を減らすことが最優先
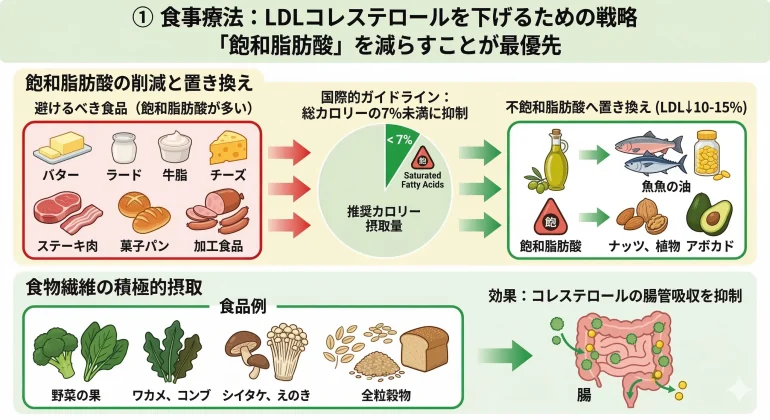
LDLコレステロールを上げる最大の食事因子は、飽和脂肪酸です。 飽和脂肪酸は、バター・ラード・牛脂・チーズ・脂身の多い肉・菓子パン・加工食品などに多く含まれています。
国際的なガイドラインでは、飽和脂肪酸のエネルギー比を総カロリーの7%未満に抑えることが推奨されています。 飽和脂肪酸を不飽和脂肪酸(オリーブオイル・魚油・ナッツ類など)に置き換えることで、LDLコレステロールを10〜15%程度低下させることが可能です。
また、食物繊維(野菜・海藻・きのこ・全粒穀物など)はコレステロールの腸管吸収を抑制する効果があり、積極的な摂取が推奨されています。
😄ちょこっと解説‼️
「卵を食べるとコレステロールが上がる」という話をよく聞きますが、実は食事中のコレステロール摂取量とLDLコレステロール値の関係は、かつて考えられていたほど単純ではありません。 LDLコレステロール値に最も影響するのは飽和脂肪酸の摂取量であり、鶏卵は適量であれば問題ないとする見解が現在では一般的です。
当院には管理栄養士が在籍しており、コレステロールを含む生活習慣病の栄養指導を行っています。
「何を食べたらいいのかわからない」 「コレステロールを下げる食事の工夫を知りたい」という方は、ぜひ当院の栄養指導外来:食サポをご利用ください。
② 運動療法: 週150分の有酸素運動
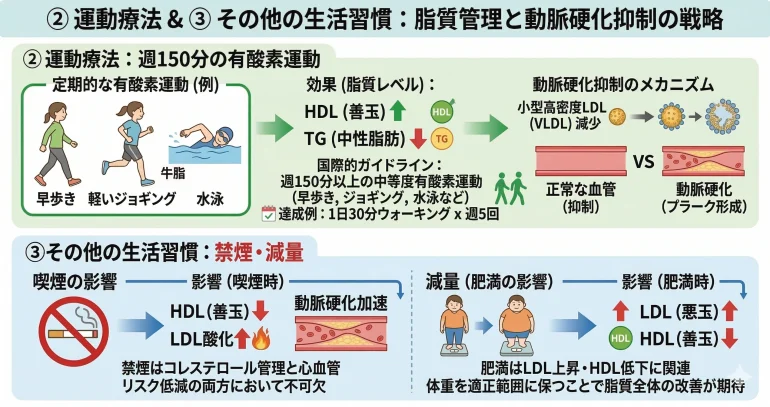
定期的な有酸素運動は、HDL(善玉)コレステロールを増加させ、TG(中性脂肪)を低下させる効果があります。 LDL(悪玉)コレステロール自体への直接的な低下効果はやや限定的ですが、運動はLDL粒子の質を改善させることができます。 すなわち、小型高密度LDL=VLDL(超悪玉)コレステロールを減少させて、動脈硬化の進行を抑制することが報告されています。
国際的なガイドラインでは、週150分以上の中等度の有酸素運動(早歩き・軽いジョギング・水泳など)が推奨されています。 1日30分のウォーキングを週5回行えば達成できます。
③ その他の生活習慣: 禁煙・減量
喫煙はHDLコレステロールを低下させ、LDLの酸化を促進し、動脈硬化を加速させます。 禁煙はコレステロール管理と心血管リスク低減の両方において不可欠です。
肥満はLDLコレステロールの上昇やHDLの低下に関連しています。 体重を適正範囲に保つことで、脂質全体の改善が期待できます。
④ 薬物治療: スタチンを中心とした段階的アプローチ
生活習慣の改善は脂質管理の基本ですが、それだけでは十分にLDLが下がらない場合、あるいは心血管リスクが高い場合には、薬物治療が必要です。 日本動脈硬化学会の「動脈硬化性疾患予防ガイドライン2022年版」(JAS 2022)に基づく治療戦略を整理します。
第1段階:スタチン: 脂質低下治療の柱
スタチンは、肝臓でのコレステロール合成を抑制する薬で、日本のガイドラインでも脂質低下治療の第一選択薬に位置づけられています。 日本で広く使用されているストロングスタチン(ロスバスタチン、アトルバスタチン、ピタバスタチンなど)は、用量に応じてLDLコレステロールを約30〜50%低下させることができます。
CTTメタ解析が示すように、LDLを約39mg/dL(1mmol/L)下げるごとに心血管イベントが約22%低下するという圧倒的なエビデンスに支えられています。 スタチンは世界で最も処方されている薬のひとつであり、その安全性と有効性は数十万人規模の臨床試験で確立されています。
第2段階:エゼチミブ: 小腸からの吸収を抑える
スタチンだけでは目標に達しない場合、エゼチミブを追加します。 エゼチミブは小腸でのコレステロール吸収を選択的に阻害する薬で、スタチンとの併用でさらに約15〜20%のLDL低下が得られます。 IMPROVE-IT試験(NEJM 2015)では、急性冠症候群後の患者でスタチン+エゼチミブの併用が、スタチン単独に比べて心血管イベントを有意に減少させることが示されました。 日本でもこの併用療法は広く行われており、JAS 2022でもスタチンで管理目標に達しない場合の重要な選択肢として位置づけられています。
第3段階:PCSK9阻害薬: LDLをさらに劇的に低下
スタチン+エゼチミブでもLDLが目標に達しない場合、PCSK9阻害薬が追加されます。 PCSK9阻害薬は、肝臓の表面にあるLDL受容体の分解を防ぐことで、血液中からLDLを効率よく回収する仕組みです。 注射薬として2〜4週に1回投与し、LDLを約50〜60%さらに低下させます。
現在日本で使用されている主なPCSK9阻害薬は、エボロクマブ(レパーサ®)とアリロクマブ(プラルエント®)の2種類です。 いずれも大規模臨床試験(FOURIER試験・ODYSSEY OUTCOMES試験)で心血管イベントの有意な減少が確認されています。 家族性高コレステロール血症や、スタチン最大耐容量+エゼチミブでも目標値に到達しない高リスク患者さんに保険適用があります。
新しい選択肢: ベンペド酸とインクリシラン
近年、さらに新しい脂質低下薬が日本でも使えるようになっています。
ベンペド酸(ネクスレトール®)は、スタチンと同じコレステロール合成経路の上流に作用する内服薬です。 スタチン不耐(筋肉痛などの副作用でスタチンが飲めない方)の患者さんにも使用でき、CLEAR Outcomes試験(NEJM 2023)ではLDLの約21%低下と心血管イベントの約13%低下が示されました。 海外のガイドラインでは、スタチン不耐の患者さんに対する単独療法としても推奨されており、今後日本のガイドラインにも治療アルゴリズムへの正式な組み込みが期待されます。
インクリシラン(レクビオ®)は、siRNA(小分子干渉RNA)技術を用いた注射薬で、肝臓でのPCSK9タンパク質の産生自体を抑制します。 初回と3カ月後に投与した後は、6カ月に1回の投与で済むため、治療の継続性が大幅に改善されます。 日本でも2024年に保険適用となり、家族性高コレステロール血症や心血管イベントリスクが高い患者さんの新たな選択肢として注目されています。
また、現在開発中の経口PCSK9阻害薬も国際的に臨床試験が進んでおり、注射が不要な次世代の治療薬として期待されています。 メタ解析では、経口PCSK9阻害薬でLDLが約48%低下することが示されています。
| 治療段階 | 薬剤 | LDL低下率 | 投与方法 |
|---|---|---|---|
| 第1段階 | スタチン(ストロングスタチン) | 約30〜50% | 毎日内服 |
| 第2段階 | +エゼチミブ | さらに約15〜20% | 毎日内服 |
| 第3段階 | +PCSK9阻害薬 | さらに約50〜60% | 2〜4週に1回注射 |
| 代替 | ベンペド酸 | 約21% | 毎日内服(スタチン不耐に) |
| 代替 | インクリシラン | 約50% | 6カ月に1回注射 |
⑤ LDLコレステロールの目標値——どこまで下げればよいのか?
日本動脈硬化学会の「動脈硬化性疾患予防ガイドライン2022年版」では、患者さんの心血管リスクに応じてLDLコレステロールの管理目標値が設定されています。 2022年版の大きな特徴は、リスク評価に久山町研究スコア(冠動脈疾患とアテローム血栓性脳梗塞を統合した絶対リスク評価)が採用されたことと、二次予防の対象にアテローム血栓性脳梗塞が正式に加えられたことです。
【一次予防(まだ心血管疾患を発症していない方)】
| リスク区分 | LDL-C管理目標値 | 主な対象 |
|---|---|---|
| 低リスク | <160mg/dL | リスク因子が少ない方 |
| 中リスク | <140mg/dL | 複数のリスク因子を有する方 |
| 高リスク | <120mg/dL | 糖尿病(末梢動脈疾患・細小血管症・喫煙なし)、CKD、 脳梗塞(アテローム血栓性以外)など |
【二次予防(すでに心血管疾患を発症した方)】
| 対象 | LDL-C管理目標値 |
|---|---|
| 冠動脈疾患・アテローム血栓性脳梗塞の既往 | <100mg/dL |
| 上記に加え:急性冠症候群、家族性高コレステロール血症、糖尿病合併、 冠動脈疾患+アテローム血栓性脳梗塞の合併 |
<70mg/dL |
2022年版で特に重要なのは、二次予防の対象にアテローム血栓性脳梗塞が加わったことです。 これは、脳卒中後の再発予防においてもLDLコレステロール管理が極めて重要であることを反映しています。 脳神経外科の立場からも、非常に意義のある改訂だと考えています。
また、糖尿病の患者さんについても細分化が進み、末梢動脈疾患や細小血管症(網膜症・腎症・神経障害)を合併している場合、あるいは喫煙のある場合は、一次予防でも100mg/dL未満というより厳格な管理が求められるようになりました。
【世界的な潮流——「もっと下げる」方向へ】
なお、2025年に改訂された欧州のESC/EASガイドラインでは、心血管イベントを繰り返すような超高リスク患者に対してLDL 40mg/dL未満という新しいカテゴリ(extreme risk)が新設されました。 日本のガイドラインはまだここまで踏み込んでいませんが、TST試験(第2章で解説)が示すように、脳卒中後の再発予防でもLDLを70mg/dL未満にすることで明確な効果が得られることが証明されています。
今後、日本のガイドラインも次の改訂では国際的なエビデンスを反映し、さらに積極的な目標設定に向かう可能性があります。 つまり、「下げれば下げるほどよい」という"the lower, the better"の考え方は、日本でも今後ますます定着していくと考えられます。
「お薬を飲み始めたら一生やめられないのでは?」と心配される方もいらっしゃいますが、これは高血圧の薬と同じ考え方です。 大切なのは、お薬を「やめること」ではなく、心筋梗塞や脳卒中を「防ぐこと」です。 生活習慣の改善で十分にLDLが下がれば、医師と相談の上で減薬できることもあります。
📖 根拠文献: 日本動脈硬化学会. 動脈硬化性疾患予防ガイドライン2022年版. 2022.
📖 Cholesterol Treatment Trialists' (CTT) Collaboration. Efficacy and safety of more intensive lowering of LDL cholesterol. The Lancet. 2010;376:1670–1681.
📖 Cannon CP, Blazing MA, Giugliano RP, et al. Ezetimibe Added to Statin Therapy after Acute Coronary Syndromes (IMPROVE-IT). N Engl J Med. 2015;372(25):2387–2397.
📖 Nissen SE, et al. Bempedoic Acid and Cardiovascular Outcomes in Statin-Intolerant Patients (CLEAR Outcomes). N Engl J Med. 2023;388(15):1353–1364.
📖 2025 ESC/EAS Focused Update on Lipid Management. Eur Heart J. 2025.
最終章 LDLコレステロールを放置しない!
ここまでお読みいただき、ありがとうございます。
このブログを通じてお伝えしたかったことは、たった一つです。
LDLコレステロールを、放置しないでください。
LDLコレステロールは「サイレント・キラー」として、自覚症状がまったくありません。 だからこそ、「数値がちょっと高いくらいなら大丈夫だろう」と放置してしまいがちです。 しかし、ここまで見てきたように、高LDLコレステロールは・・・
- 心筋梗塞・狭心症の最大のリスク因子のひとつです。 LDLを約39mg/dL(1mmol/L)下げるごとに心血管イベントが約22%低下します。
- アテローム血栓性脳梗塞の原動力です。 頚動脈や脳動脈のプラーク形成にLDLが直接関与し、TST試験ではLDL<70mg/dLへの管理で脳卒中再発リスクが22%低下しました。
- 認知症の新たな修正可能リスク因子です。 2024年Lancet委員会は、全認知症の約7%が中年期の高LDLに起因すると推定しました。
- 閉塞性動脈硬化症(PAD)の主要リスク因子です。 足の血管が詰まるだけでなく、全身の動脈硬化を示す「警報」でもあります。
- さらに、大動脈弁狭窄症・腎動脈硬化症など、全身のあらゆる動脈硬化性疾患に関与しています。
しかし、LDLコレステロールには「修正可能」という大きな希望があります。
食事の見直し・運動・禁煙という生活習慣の改善は、エビデンスに裏付けられた確実な予防策です。 そして、スタチン・エゼチミブ・PCSK9阻害薬・ベンペド酸・インクリシランなど、LDLを劇的に下げる薬物治療の選択肢は、かつてないほど充実しています。
LDLコレステロールを放置することは、「心筋梗塞・脳梗塞・認知症状態への招待状」を受け取り続けることに等しいのです。 逆に、今日からLDLの数値を意識し、管理を始めることは、将来の自分の脳と心臓と体を守る、最も確実な投資です。
当院では、脳神経外科専門医・脳卒中専門医として、LDLコレステロールと脳卒中・認知症の関連を熟知した上で、脂質管理からMRIによる脳血管の評価、管理栄養士による栄養指導まで、包括的な診療を行っています。 「コレステロールが高いと言われた」 「脳卒中が心配」 「認知症を予防したい」・・・そんな方は、ぜひ一度ご相談ください。 あなたの脳の健康の生涯パートナーとして、私たちはお手伝いいたします。
あづま脳神経外科リハビリクリニック 大阪市天王寺区生玉前町2-6
生活習慣病外来のご案内 栄養指導のご案内 脳卒中外来のご案内 認知症外来のご案内
よくある質問(FAQ)
Q. LDLコレステロールが高いと、どんな症状が出ますか?
A. 残念ながら、LDLコレステロールが高いだけでは自覚症状はほとんどありません。 これが最も恐ろしい点です。 症状が出るのは、動脈硬化が進行して心筋梗塞(胸の痛み)、脳梗塞(手足の麻痺・ろれつが回らない)、閉塞性動脈硬化症(歩くと足が痛い)などが発症したときです。 症状が出る前に健康診断で発見し、治療を開始することが極めて重要です。
Q. LDLコレステロールの正常値はいくつですか?
A. 一般にLDL 140mg/dL以上が「高LDLコレステロール血症」、120〜139mg/dLが「境界域」とされています。 ただし、心血管リスクが高い方(脳梗塞・心筋梗塞の既往がある方、糖尿病がある方など)では、70mg/dL未満、さらに高リスクの方は55mg/dL未満が目標となります。 目標値は個人のリスクによって異なりますので、主治医にご相談ください。
Q. スタチン(コレステロールの薬)の副作用が心配です。
A. スタチンの最も多い副作用は筋肉痛(ミオパチー)で、報告によって差がありますが臨床試験では5〜10%程度に認められました。 重篤な横紋筋融解症は非常にまれです(10万人あたり数件)。 近年では、スタチン不耐の方にはベンペド酸やPCSK9阻害薬など代替薬があります。 副作用のリスクよりも、心筋梗塞や脳梗塞を予防するメリットの方がはるかに大きいことが、数十万人規模の研究で示されています。 副作用が気になる方は、自己判断で中止せず、必ず主治医にご相談ください。
Q. 食事だけでLDLコレステロールは下がりますか?
A. 食事療法だけでLDLコレステロールを10〜15%程度低下させることは可能です。 特に、飽和脂肪酸(バター・脂身の多い肉・加工食品など)を減らし、不飽和脂肪酸(魚・オリーブオイル・ナッツなど)や食物繊維を増やすことが有効です。 ただし、LDLコレステロールの約7割は肝臓で合成されており、食事の影響には限界があります。 心血管リスクが高い方は、食事療法に加えて薬物治療が必要になることが多いです。
Q. LDLコレステロールが認知症のリスクになると聞きました。何歳から気をつければいいですか?
A. 2024年のLancet委員会報告書では、40歳頃から高LDLコレステロールの検出と治療を開始することが推奨されています。 全認知症の約7%が中年期の高LDLに起因すると推定されており、これは14のリスク因子の中で難聴と並んで最も大きい寄与率です。 40代のうちから定期的に脂質検査を受け、必要に応じて治療を開始することが、将来の認知機能を守る上で重要です。
Q. あづま脳神経外科リハビリクリニックではLDLコレステロールの治療をしてもらえますか?
A. はい。 当院では、脳神経外科専門医・脳卒中専門医の立場から、LDLコレステロールと脳卒中・認知症の関連を踏まえた総合的な脂質管理を行っています。 脳のMRI検査による脳血管・頚動脈の評価、管理栄養士による栄養指導、脂質低下薬の処方と調整、リハビリテーションスタッフによる運動指導まで、包括的なサポートを提供しています。
参考文献
- Borén J, Chapman MJ, Krauss RM, et al. Low-density lipoproteins cause atherosclerotic cardiovascular disease: pathophysiological, genetic, and therapeutic insights: a consensus statement from the European Atherosclerosis Society Consensus Panel. Eur Heart J. 2020;41(24):2313–2330.
- Ference BA, Ginsberg HN, Graham I, et al. Low-density lipoproteins cause atherosclerotic cardiovascular disease. 1. Evidence from genetic, epidemiologic, and clinical studies. A consensus statement from the EAS Consensus Panel. Eur Heart J. 2017;38(32):2459–2472.
- Cholesterol Treatment Trialists' (CTT) Collaboration. Efficacy and safety of more intensive lowering of LDL cholesterol: a meta-analysis of data from 170,000 participants in 26 randomised trials. The Lancet. 2010;376(9753):1670–1681.
- Sabatine MS, Giugliano RP, Keech AC, et al. Evolocumab and Clinical Outcomes in Patients with Cardiovascular Disease (FOURIER). N Engl J Med. 2017;376(18):1713–1722.
- Schwartz GG, Steg PG, Szarek M, et al. Alirocumab and Cardiovascular Outcomes after Acute Coronary Syndrome (ODYSSEY OUTCOMES). N Engl J Med. 2018;379(22):2097–2107.
- Nicholls SJ, et al. Evolocumab in Patients without a Previous Myocardial Infarction or Stroke (VESALIUS-CV). N Engl J Med. 2025.
- Amarenco P, Kim JS, Labreuche J, et al. A Comparison of Two LDL Cholesterol Targets after Ischemic Stroke (Treat Stroke to Target). N Engl J Med. 2020;382(1):9–19.
- Livingston G, Huntley J, Liu KY, et al. Dementia prevention, intervention, and care: 2024 report of the Lancet standing Commission. The Lancet. 2024;404(10452):572–628.
- Imamura T, Doi Y, Arima H, et al. LDL Cholesterol and the Development of Stroke Subtypes and Coronary Heart Disease in a General Japanese Population: The Hisayama Study. Stroke. 2009;40(2):382–388.
- Zhong P, Wu S, Feng R, et al. The Global Burden of Diseases attributed to high low-density lipoprotein cholesterol from 1990 to 2019. BMC Public Health. 2022;22:1903.
- Global Burden of Disease Study 2023. Burden of 375 diseases and injuries, risk-attributable burden of 88 risk factors, 1990–2023. The Lancet. 2025;405(10498).
- Cannon CP, Blazing MA, Giugliano RP, et al. Ezetimibe Added to Statin Therapy after Acute Coronary Syndromes (IMPROVE-IT). N Engl J Med. 2015;372(25):2387–2397.
- Nissen SE, et al. Bempedoic Acid and Cardiovascular Outcomes in Statin-Intolerant Patients (CLEAR Outcomes). N Engl J Med. 2023;388(15):1353–1364.
- Song P, Rudan D, Zhu Y, et al. Global, regional, and national prevalence and risk factors for peripheral artery disease in 2015. Lancet Glob Health. 2019;7(8):e1020–e1030.
- 2025 ESC/EAS Focused Update on Lipid Management. Eur Heart J. 2025.
免責
本記事は一般的な医学情報の提供を目的としています。 症状や治療は個人差があるため、心配な方は医療機関へご相談ください。
急に手足が動かなくなった、ろれつが回らない、激しい頭痛がある、意識がもうろうとするなどの症状があれば、すぐに救急車を呼んでください。
この記事の監修医師 当院院長 我妻 敬一(あづま けいいち)
医療法人 華拓昇会 あづま脳神経外科リハビリクリニック
〒543-0072 大阪市天王寺区生玉前町2-6
専門医資格: 脳神経外科専門医/脳卒中専門医
所属学会: 日本脳神経外科学会、日本頭痛学会、日本脳卒中学会、日本認知症学会など
我妻院長の専門領域: 脳卒中、片頭痛、認知症、しびれ、ふらつき、坐骨神経痛
当院の特徴: 当日MRI検査、専門医診療、神経難病外来、脊椎外来、脳卒中・神経難病リハビリ、栄養指導







